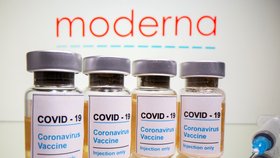
Vakcína Moderny má v EU zelenou, do Česka může dorazit 22. ledna. Děti ale mají smůlu
Evropská komise dnes schválila podmínečnou registraci vakcíny firmy Moderna v zemích Evropské unie. Unijní exekutiva oznámila povolení již druhé očkovací látky proti covidu-19 v tiskové zprávě. Členské státy budou mít spolu s vakcínou firem Pfizer a BioNTech, kterou již začaly všechny země používat, k dispozici celkem 460 milionů dávek. EU má dalších jeden a půl miliardy dávek nasmlouváno u dalších čtyř výrobců, jejichž přípravky na schválení teprve čekají. Vakcína už může zamířit i do Česka, kam by první dodávka mohla dorazit 22. ledna.
„Tato vakcína nám dává další nástroj k překonání současné krize,“ komentovala podmínečné doporučení druhé očkovací látky šéfka Evropské lékové agentury Emer Cookeová.
EMA bude podle ní nadále monitorovat údaje o bezpečnosti a efektivitě této vakcíny, které jí musí výrobce poskytovat. Agentura doporučila aplikaci vakcíny pro pacienty starší 18 let, zatím tak nebude určená pro děti.
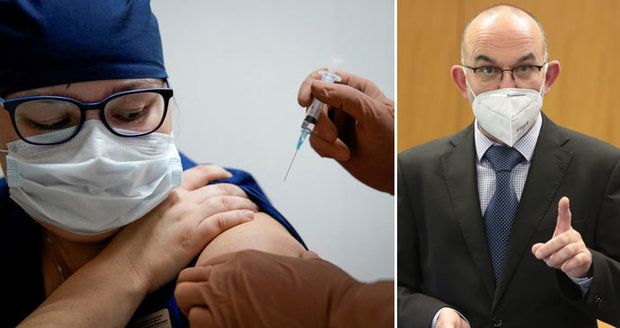
Šéfka SÚKL: Do ČR přijde další bezpečná vakcína
„Další dostupná očkovací látka - skvělá zpráva a skutečnost, která nás přibližuje k běžnému životu. Děkuji pracovníkům SÚKL, kteří se na jednáních EMA podíleli, díky nim víme, že do České republiky přijde prověřená a bezpečná vakcína,“ uvedla v reakci ředitelka SÚKL Irena Storová.
Ústav přitom poznamenává, že vakcína v klinickém hodnocení prokázala 94,1% účinnost.
„Klinické hodnocení rovněž prokázalo 90,9% účinnost u pacientů s rizikem rozvoje závažného průběhu onemocnění COVID-19, včetně pacientů s chronickým onemocněním plic, srdečním onemocněním, obezitou, onemocněním jater, diabetem nebo infekcí HIV,“ popisuje SÚKL.
I v případě aplikace této vakcíny se stejně - jako při jiných očkováních - mohou dostavit vedlejší účinky. Mezi nejběžnější vedlejší účinky očkování patří bolest či otok v místě vpichu, únava, malátnost, zvýšená teplota či bolení hlavy.
Kritika za nedostatek vakcín
Evropská komise v posledních dnech čelila kritice politiků z některých zemí, podle nichž nezajistila dostatek látek pro co nejrychlejší distribuci.
Komise to odmítla s odůvodněním, že problém je v současnosti hlavně v nedostatečných výrobních kapacitách. Unijní státy začaly od konce loňského roku různým tempem očkovat první schválenou látkou, které by měly do konce září dostat celkem 300 milionů dávek. Po schválení komisí budou moci začít využívat i druhou vakcínu, které pro ně Brusel v loni podepsané smlouvě zajistil 160 milionů dávek.
Do Česka by přibližně od března měly postupně zamířit až tři miliony dávek této látky. „Nyní v plném tempu pracujeme na schválení (vakcíny) a jejím zpřístupnění pro EU,“ uvedla po rozhodnutí EMA předsedkyně komise Ursula von der Leyenová. Eurokomisařka pro zdravotnictví doplnila, že komise vakcínu schválí „zanedlouho“.
Výhoda oproti Pfizeru: Nejsou třeba teploty -70°C
Látka společnosti Moderna má proti přípravku firem Pfizer a BioNTech výhodu v tom, že nemusí být skladována při extrémně nízkých teplotách, a bude proto jednodušší ji distribuovat až k samotným pacientům. I tato vakcína by se ovšem pro maximální ochranu podávala ve dvou dávkách, přičemž druhé očkování se má provádět čtyři týdny po prvním.
Účinnost očkovací látky okolo 95 procent podle EMA potvrdilo testování s účastí 30.000 lidí. Protože byla vakcína schválena podmínečně, musí její výrobce průběžně v následujících dvou letech dodávat další klinická data. Další testy by měly mimo jiné prokázat, jak dlouho vakcína chrání před covidem-19, jak dobře brání závažnému průběhu nemoci, jak účinně chrání pacienty s oslabenou imunitou, děti a těhotné ženy či zda dokáže zabránit i případům nemoci bez příznaků.




















Buďte první, kdo se k tématu vyjádří.